راهکارهای تغذیه ای برای بهینه کردن سیستم ایمنی گاوهای شیری

چکیده
با افت عملکرد سیستم ایمنی، گاوهای شیری در حول و حوش زایمان مستعد افزایش وقوع و شدت بیماری های متابولیک و عفونی می باشند. عامل سهیم مهم در افزایش اختلالات سلامت، تغییرات در مکانیسم سیستم ایمنی گاوها است. حقیقتاً، التهاب کنترل نشده یکی از عوامل سهیم و یک عامل مرتبط بین چند بیماری متابولیکی و عفونی مهم اقتصادی نظیر ورم پستان، جفت ماندگی، متریت، جابه جایی شیردان و کتوز می باشد.
وضعیت تغذیه ای گاوهای شیری و متابولیسم مواد مغذی خاص، تنظیم کننده های بحرانی عملکرد سلول های ایمنی می باشند. امروزه درک بیشتری وجود دارد که واسطه های خاصی از سیستم ایمنی می توانند اثر متقابلی را روی متابولیسم مواد مغذی دارا باشند. بنابراین، هر گونه اختلالاتی در تغذیه یا هموستاز ایمنی می تواند بازخورد های (فیدبک های) آسیب رسانی را به وجود آورد که این خود می تواند افزایش بیشتر اختلالات سلامت، افزایش افت تولید و کاهش در دسترس پذیری ایمن و مواد خوراکی لبنی را برای جمعیت رو به رشد جهان فراهم کند.
این مقاله ارتباطات پیچیده بین متابولیسم مواد مغذی و عملکرد سیستم ایمنی در گاوهای حول و حوش زایمان را به بحث خواهد گذاشت. جزئیات چگونگی کمبود و بیش بود مواد مغذی میکرو و ماکرو که میتواند در اختلال عملکرد سیستم ایمنی و متعاقب آن توسعه اختلالات سلامت تأثیر بگذارد، ارائه خواهد شد. به طور مشخصی، راه هایی که متابولیسم مواد مغذی و تنش اکسیداتیو را تغییر می دهند، می توانند سیستم ایمنی را در گاوهای انتقالی به مخاطره اندازند که در مورد آن بحث خواهد شد. درک بهتر ارتباط بین تغذیه و سیستم ایمنی می تواند طراحی جیره های غذایی را تسهیل کرده که این خود حساسیت به بیماری را در گاوهای اوایل شیردهی کاهش خواهد داد.
مقدمه
بیماری دام ها یک عامل بازدارنده در سود دهی و دامپروری پایدار است. گاوهای شیری به طور خاصی در طول دوره حول و حوش زایمان نسبت به افزایش وقوع و شدت بیماری های متابولیکی و عفونی حساس هستند. مشکلات سلامت رخ داده در پیرامون زمان زایش به طور خاصی مسئله ساز هستند، زیرا به طور قابل توجهی بازده تولیدی گاوها را در دوره شیرواری بعدی تحت تأثیر قرار میدهند.
زیانهای اقتصادی مستقیم مرتبط با اختلالات سلامتی حول و حوش زایش شامل: کاهش ظرفیت تولیدی گاو و افزایش نرخ مرگ و میر می باشد. ضررهای اقتصادی غیر مستقیم مرتبط با بیمارهای گاو شامل: هزینه داروهای ضد میکروبی، واکسیناسیون، ضوابط نگهداری و کارگری مورد نیاز برای انجام درمان و کنترل بیماری می باشد.
بخشی از توانایی گاو شیری در مقاومت برابر ایجاد بیماری در طول دوره حول و حوش زایمان با بازده سیستم ایمنی مرتبط است. سیستم ایمنی حاوی طیفی از اجزا و فرآیندهای بیولوژیکی است که دام ها را در برابر پیامدهای بیماری ها محافظت می کند. نقش اصلی سیستم ایمنی پیشگیری از تهاجم میکروبی به بدن، رفع عفونت های موجود و دیگر منابع آسیب سلولی و بازیابی بافتها در جهت عملکرد طبیعی می باشد. در گاوهای شیری، سیستم ایمنی یک شبکه چند منظورهای از عوامل فیزیکی، سلولی و محلول را در تسهیل دفاع در برابر مجموعه متنوعی از چالش های میکروبی بکار می گیرد. این سیستم یکپارچه مکانیسم دفاعی به طور قابل توجهی در حفظ تعادل ظریف بین فعال سازی ایمنی مورد نیاز برای پیشگیری از بیماری و حل و فصل فعالیت در زمان پایان تهدید مهاجم تنظیم می شود.
این مقاله مروری خلاصه ای از سیستم ایمنی گاو را فراهم و نحوه پاسخ ایمنی کمتر از حد مطلوب را تشریح خواهد کرد که ممکن است در برابر بیماری به شکست انجامد، ارتباط بین تغذیه و عملکرد ایمنی را تشریح خواهد شد و راهکارهای کنونی برای پاسخ مطلوب سیستم ایمنی در گاوهای شیری در زمان هایی که حساسیت به بیماری افزایش می یابد را توضیح می دهد. با توجه به نقش بحرانی که تغذیه در حمایت از عملکرد کلی ایمنی ایفا می کند، بایستی راهکارهای مدیریتی مبتنی بر تغذیه یک نقش کلیدی را در هر برنامه پیشگیری از بیماری داشته باشد.
مرور کلی بر سیستم ایمنی
سیستم ایمنی بایستی گاو شیری را از انواع ارگانیسم های بیماری زا مثل ویروس ها، باکتری ها و انگل ها محافظت کند. برای انجام این کار سیستم ایمنی یک شبکه پیچیده و دینامیکی از بافتها، سلولها و مولکولهایی (که می توانند به دو دسته مجزا تقسیم شوند: ایمنی ذاتی و ایمنی اکتسابی) را به کار می گیرد.
سیستم ایمنی ذاتی با پاسخ اولیه و سریع مشخص می شود که می تواند در عرض چند ثانیه به دنبال التهاب اولیه بافت رخ دهد. ایمنی ذاتی در دامنه ای با ظرفیت پاسخ به هر بافت آسیب دیده یا خنثی سازی طیف وسیعی از پاتوژن ها توسعه می یابد. ایمنی اکتسابی در مقایسه با ایمنی ذاتی با تأخیر رخ داده و می تواند چندین روز طول بکشد. ایمنی اکتسابی یک واکنش سفارشی و خاص به پاتوژن های عفونی است و می تواند با مواجهه مکرر میکروب های مشابه تقویت شود.
در مجموع، سیستم های ایمنی ذاتی و اکتسابی باید به طور هماهنگ برای فراهم کردن حفاظت بهینه از تهدیدات خارجی و بقای گاو عمل کنند. بررسیهای قبلی توضیحاتی از سیستم ایمنی گاو در زمان حول و حوش زایش را ارائه میدهند (Mallard et al., 1998; Sordillo and Streicher, 2002;Aitken et al., 2011). لذا این بررسی تنها خلاصه ای از اجزای اصلی ایمنی گاو شیری با تأکید بیشتر بر نحوه تأثیر گذاری وضعیت تغذیه ای و مواد مغذی ویژه بر جنبه های اساسی دفاع میزبان را فراهم می کند.
ایمنی ذاتی
در بیشتر موجودات زنده سیستم ایمنی ذاتی، مکانیسم دفاعی غالب میزبان می باشد. ایمنی ذاتی شامل اجزای غیر اختصاصی سیستم ایمنی است که می تواند به کل میکروب های عفونی پاسخ دهد. اجزاء ایمنی ذاتی اولین خط دفاعی در برابر پاتوژن های مهاجم است زیرا آنها همواره آماده بوده و به سرعت در محل فعال می شوند. بسته به بازدهی دفاع ذاتی، میکروب ها می توانند در عرض چند دقیقه تا ساعت ها بعد از حمله از بین بروند. این خط اولیه دفاعی می تواند خیلی سریع و کار آمد باشد که تغییرات قابل توجهی را در عملکرد فیزیولوژیک طبیعی بافت ها به عنوان یک نتیجه از حمله میکروبی ایجاد نمی کند.
به دلیل ماهیت غیر اختصاصی، مکانیسم ایمنی ذاتی با در معرض قرار گیری مجدد عوامل مشابه تقویت نمی شود. اجزاء اصلی سیستم ایمنی ذاتی شامل سدهای مکانیکی و فیزیکی، فاگوسیتها، اندوتلیوم عروقی و واسطههای محلول مختلف حاصل از جمعیت-های سلولی مختلف تحت تأثیر قرار گرفته در داخل بافتها می باشند (جدول 1). سدهای مکانیکی و فیزیکی برای پیشگیری از ورود پاتوژن ها به بدن ضروری هستند. بعضی نمونه های دفاعی سدهای سطحی که مانع از حمله میکروبی می شوند شامل: پوست، اشک ها و موکوس. زمانی که پاتوژن ها توانستند از این خط دفاعی عبور کنند، سلول ها و اجزاء محلول ایمنی ذاتی بایستی سریعاً برای جلوگیری از ایجاد بیماری پاسخ دهند.
گیرندههای شناسایی الگو (PRR) نقش مهمی برای درک حضور پاتوژن های مهاجم عبور کرده از سدهای دفاعی در ایمنی ذاتی دارند. این گیرنده ها در تشخیص طیفی از عوامل میکروبی مرتبط با عفونت عمل می کنند و می توانند روی سطوح سلول ها بیان شده، ترشح شود و یا در داخل سلول بیان گردد (Jungi et al., 2011;Kumar et al., 2011). اولین گیرنده شناسایی الگوی (PRR) شناخته شده، تول (Toll) در مگس سرکه بود و امروزه گیرنده شبه تول (TLR) بین اکثر پژوهش های انجام شده روی PRR، در پستانداران هستند (Kawai and Akira, 2011). حداقل ده TLR مختلف گاوی شناسایی شده اند و می توانند به طیفی از محصولات میکروبی و لیگاندهای درون زادی که مجموعاً الگوهای مولکولی وابسته به پاتوژن (PAMP)( McGuire et al., 2006) نامیده می شوند، متصل گردند. بعضی از الگوهای مولکولی وابسته به پاتوژن (PAMP) که منحصر به فرد هستند به گروه های خاصی از میکروب ها مثل لیپوپپتیدهای باکتری های گرم مثبت و لیپوپلی ساکاریدهای باکتری های گرم منفی اختصاص دارند (Jungi et al., 2011;Kumar et al., 2011).
| عامل | عملکردهای اصلی |
|---|---|
| سدهای فیزیکی | بلوکه کردن و به دام انداختن میکروب ها (پوست، اشک، مخاط) |
| گیرنده های شناسایی الگو | مراقبت و فعال سازی پاسخ های ایمنی ذاتی |
| سیستم کمکی | عمل باکتریولایتیک و فاگوسیتوز را تسهیل می کند. |
| سیتوکین ها | ایمن سازی برای ایمنی ذاتی و ایمنی اکتسابی |
| اکسی لیپیدها | شروع کننده و اتمام التهاب |
| سلول های اندوتلیال | تنظیم مهاجرت لکوسیت ها و فعال سازی آنها |
| نوتروفیل ها | فاگوسیتوز، آنزیم های ضد باکتریایی، پپتیدهای دفاعی (دفنسین ها) و گونه های اکسیژن واکنش پذیر، شکل گیری تله خارج سلولی نوتروفیل (NET) |
| ماکروفاژها | فاگوسیتوز، تولید سیتوکین ها و اکسی لیپیدها |
| سلول های دندریتیک | فاگوسیتوز، ارتباط ایمنی ذاتی و اکتسابی |
| سلول های کشنده طبیعی | هدف و کمک به از بین بردن عفونت سلول های میزبان |
جدول 1- اجزای سیستم ایمنی ذاتی
نمونه هایی از گیرندههای شناسایی الگوی یافت شده در سلول های ایمنی و غیر ایمنی که میتواند طیف وسیعی از الگوهای مولکولی وابسته به پاتوژن را شناسایی کنند شامل مجموعه تمایزی 14، گیرندههای الیگومریزاسیون شبه دامین متصلشونده به نوکلئوتید و خانواده TLR مثل: TLR2، TLR4، TLR5 و TLR9. گیرنده های شناسایی الگو (PRR) بعد از اتصال به لیگاندهایشان می توانند آبشارهای سیگنال داخل سلولی را شروع کنند که منجر به آغاز پاسخ های ایمنی ذاتی یا می-توانند مستقیماً فعالیت ضد میکروبی را تسهیل کنند (Kumar et al., 2011).
زمانی که میکروب ها به بافت های میزبان هجوم می آورند با چندین عامل محلول دفاع داخلی ایمنی ذاتی مواجه می شوند. بسته به محل حمله، بعضی از این عوامل محلول می توانند از طریق سیگنال دهی آبشاری بعد از شناسایی عوامل میکروبی توسط گیرنده های شناسایی الگوی روی سلولهای میزبان تولید شوند.
به عنوان مثال سیستم کمکی جزئی از سیستم دفاع ذاتی است که دارای مجموعه ای از پروتئین های موجود در سرم و دیگر مایعات بدن می باشد که می تواند با دیگر واسطه های ایمنی مانند سیتوکین ها به منظور تقویت مکانیسم های ضد میکروبی ارتباط برقرار کند (Hajishengallis and Lambris, 2010). پروتئین های درگیر در سیستم کمکی به طور عمده توسط هپاتوسیت ها ساخته می شوند، اما دیگر منابع سلولی شامل مونوسیت ها و ماکروفاژهای بافتی می باشند. آبشار کمکی شامل چندین مولکول مؤثر مختلف نظیر عوامل کمکی C3، C5a و کمپلکس C5b-9 است (Hajishengallis and Lambris,2010).
فعال سازی سیستم کمکی می تواند منجر به فعالیت های ضد باکتریایی مستقیم حاصل از نشستن مولکول های تشکیل دهنده منافذ بر روی باکتری شود. دیگر عملکردهای بیولوژیکی مهم سیستم کمکی که در کشتن میکروب ها سهیم هستند شامل توقف باکتری ها یا شروع و فعال ساختن سلول های ایمنی میزبان برای فاگوسیتوز و کشتار داخل سلولی. سیستم کمکی همچنین مسئول جذب شیمیایی قوی برای بکارگیری و فعال سازی سلول های التهابی (نوتروفیل ها و مونوسیت ها) در زمان اوایل عفونت است (Rainard, 2003). سیستم کمکی مثل TLR قادر به شناسایی ساختارهای میکروبی محافظت شده نظیر اجزای دیواره سلولی و اشکال کربوهیدراتی از طریق روش شناسایی الگو می باشد (Hajishengallis and Lambris, 2010).
سیتوکین ها یک مثال عالی از دفاع ذاتی محلول هستند که به صورت پویا در نتیجه فعال سازی گیرنده های شناسایی الگو توسط PAMP القاء به تولید می شوند. برای مثال LPS یک PAMP قوی است که می تواند به TLR4 به صورت کمپلکس با CD14 و پروتئین باند کننده LPS باند شود. فعال شدن TLR4 می تواند منجر به القاء چندین مسیر التهابی نظیر: پروتئین کیناز فعال شده با میتوژن و عامل هسته ای κB (NFκB) سیگنال دهنده آبشاری شود که این خود بیان سیتوکین ها را افزایش داده و پاسخ اصلی به شمار می آید (Takeuchi and Akira, 2010).
شبکه سیتوکین شامل گروه متنوعی از پروتئین های تولید شده توسط سلول های ایمنی و غیر ایمنی در سراسر بدن و تحت شرایط مختلف است. ظرفیت ایمنولوژیک و ایمنی شبکه سیتوکین پیچیده است. تک تک سیتوکین ها قادرند با دیگر سیتوکین ها به طور سینرژیک و یا به طور آنتاگونیستی روی چند سلول هدف ارتباط برقرار کنند. سیتوکین های مختلف علاوه بر ارتباطات قابل توجهی که در شبکه سایتوکینی دارند، قادرند فرآیندهای بیولوژیک را به روش های مشابهی تحت تأثیر قرار دهند.
برای مثال فاکتور نکروز دهنده تومور آلفا (TNFα) و IL1β به سرعت در زمان های اولیه عفونت بیان می شوند و دارای عملکردهای پیش التهابی قوی می باشند، در حالیکه IL4، IL10 و IL17 به طور فعالی به خاتمه آبشار التهابی کمک می کنند (Bannerman, 2009). بیشتر سیتوکین ها عمر بسیار کوتاهی دارند، بنابراین ساخت و عملکرد آنها معمولاً در اوج فعالیت ایمنی رخ می دهد. سیتوکین ها قادرند عملکرد سلولی را ازطریق گیرنده های با میل ترکیبی بالایی که برای هر سیتوکین در سلول میزبان قرار دارد، تحت تأثیر قرار دهند.
بنابراین فعالیت هر سلول پاسخ دهنده نه تنها به کمیت و نوع سیتوکین بستگی دارد بلکه به بیان نسبی گیرنده های سیتوکین نیز وابسته است (Sordillo and Streicher, 2002; Bannerman, 2009). با توجه به ایمنی ذاتی، سیتوکین ها اثرات متنوع خودشان را با شروع پاسخ های التهابی و تسهیل مهاجرت لوکوسیتها از خون به بافت های عفونی پس از تشخیص باکتری توسط جمعیت های سلولی موضع، اعمال می کنند (Ryman et al., 2015a). الگوی بیان سیتوکین توسط سلول های بدن متفاوت است و به نوع پاتوژنی که سبب پاسخ شده بستگی دارد. به طور کلی باکتری های گرم منفی در مقایسه با باکتری های گرم مثبت مقادیر بیشتری از پاسخ های پیش التهابی سیتوکین ها را آغاز می کنند (مثل IL1، IL6، IL8 و TNFα)، باکتری های گرم مثبت به بیان ضعیف تر و پاسخ کندتر سیتوکین در زمان اوایل دوره عفونت تمایل دارند (Bannerman, 2009).
اکسی لیپیدها گروه دیگری از مولکول های سیگنال دهنده مهم سیستم ایمنی هستند که از لیپیدهای سلولی مشتق شده اند و در ایمنی ذاتی تنظیم کننده شروع، اندازه و طول پاسخ التهابی می باشند. اکسی لیپیدها از سوبسترا های PUFA ساخته می شوند که به طور عمده در غشاء سلولی نظیر لینولئیک اسید (امگا-6)، آراشیدونیک اسید یا 3-n ایکوزاپنتاانوئیک اسید (EPA) و دکوزاهگزاانوئیک اسید (DHA) یافت می شوند.
این سوبستراهای اسیدهای چرب توسط گونه های فعال اکسیژن (ROS) بدون آنزیم یا از طریق مسیرهای آنزیمی مختلف شامل سیکلواکسیژنازها (COX)، لیپواکسیژنازها (LOX) و مسیرهای سیتوکروم 450P که تولید کننده طیفی از اکسی لیپیدهایی نظیر پروستاگلاندینها (PG)، ترومبوکسان ها (TX)، لوکوتراین ها (LT) و لیپوکسین ها اکسید می شوند. بسته به زمان و میزان بیان اکسی لیپیدها می توانند هم پاسخ التهابی را خاتمه و هم افزایش دهند (Serhan et al., 2008; Sordillo and Raphael, 2013). بنابراین توازن تولید بین اکسی لیپیدهای پیش التهابی و ضد التهابی عاملی است که فنوتیپ التهابی یک سلول و محیط اطرافش را تعیین می کند.
التهاب
التهاب یک جزء مهم سیستم دفاعی ذاتی است و شامل مجموعه ای از پاسخ های بیولوژیکی سلولی و عوامل محلول در پی آسیب بافتی یا تروما است. هدف از پاسخ های التهابی میزبان، برطرف نمودن منشأ آسیب بافتی، بازگردانی هموستازی ایمنی و برگشت عملکرد طبیعی به بافت ها می باشد. آبشار التهابی نه تنها منجر به تشدید عوامل ضد میکروبی موضعی می شود بلکه حرکت لوکوسیتها و اجزای پلاسمایی از خون به بافت های عفونی را افزایش می دهد (Aitken et al., 2011; Ryman et al., 2015a). علائم بالینی التهاب شامل: قرمزی، دمای بالا، تورم و درد می باشد. این علائم بالینی را می توان با تغییرات متمایز پاسخ های اندوتلیال عروق تشریح کرد. برای مثال قرمزی، دمای بالا و درد که با افزایش جریان خون به عنوان یک پیامد ناشی از افزایش قطر عروق میباشد، افزایش نفوذ پذیری عروق ناشی از جدایی سلول های اندوتلیال متصل به هم در رگ های خونی که این مکانیسم منجر به خروج مایعات و پروتئین ها از خون و تجمع در بافت ها می شود. این رویدادها منجر به تورم و ادم مربوط به التهاب میشود (Ryman et al., 2015a).
علاوه بر تغییرات در جریان خون، اندوتلیال عروق به شکل یک دروازه بان عمل می کند وحرکت لوکوسیتها از رگ های خونی به بافت های آسیب دیده را تنظیم می کند. جمعیت سلولهای ایمنی و غیر ایمنی می توانند با PAMP و سپس آزادسازی انواع واسطه های التهابی نظیر سیتوکین ها و اکسی لیپیدهایی که آبشار التهابی را آغاز می کنند، فعال شوند. این واسط های التهابی مستقیماً روی اندوتلیوم عروق عمل می کنند تا موجب کاهش سرعت جریان خون همراه و افزایش بیان مولکول های چسبنده بر روی سلول های اندوتلیال شوند (Ryman et al., 2015a). مولکولهای چسبندهی روی لکوسیتها به مولکولهای چسبنده عروق متصل میشوند تا مهاجرت لکوسایت ها از خون به محل آسیب دیده تسهیل شود (Maddox et al., 1999; Hodgkinson et al., 2007).
نوتروفیل ها نوعی سلول غالب هستند که طی مراحل اولیه التهاب تحت تأثیر فرآیند دیاپدز (diapedesis) قرار میگیرند. در ابتدا نوتروفیل ها مهاجرت کرده و سپس به اندوتلیوم نزدیک محل عفونت متصل می شوند. سیتوکینها، اکسی لیپیدها و دیگر مولکول های واسط، حرکت نوتروفیل های چسبنده را بین سلول های اندوتلیال و عبور آن به غشای پایه نواحی بافتی آسیب دیده را تحریک می کنند. حرکت نوتروفیل ها به داخل بافت ها با گرادیان کموستاتیک ایجاد شده توسط مولکول های واسط التهابی در موضع عفونت تسهیل می شود. مهاجرت نوتروفیل ها می تواند خیلی سریع رخ داده و تقریباً 30 تا 60 دقیقه پس از آسیب در بافت ها تجمع مییابند (Summers et al., 2010).
جمعیت لوکوسیتها برای حذف پاتوژنهای میکروبی با هم همکاری میکنند. ماکروفاژها در داخل بافتها در پاسخ به هجوم باکتریها با آزاد سازی سیتوکین های تنظیم کننده ایمنی و اکسی لیپیدها تجمع می یابند. ماکروفاژها، سلول های دندریتیک و نوتروفیل های تازه کار جهت بیگانه خواری و کشتن میکروب های مهاجم عمل می کنند. فرآیند فاگوسیتوز شامل ورود باکتری به فاگوزوم هایی است که حاوی ROS ضد باکتری و آنزیم های هیدرولایتیک می باشند. ROS های حاصل از فعالیت انفجار تنفسی در فعال سازی NADPH اکسیداز و در نتیجه تولید رادیکالهای سوپر اکسید و پر اکسید هیدروژن درگیر میشوند (Babior,1999).
میلوپراکسیدها می توانند پراکسید هیدروژن را بیشتر با کلر ترکیب و هیپوکلریت تولید کرده که با فعالیت باکتریایی ارتباط دارد. علاوه بر فاگوسیتوز، نوتروفیل ها قادرند باکتری ها را از طریق مکانیسم های خارج سلولی از بین ببرند. نوتروفیل های فعال شده می توانند تله های خارج سلولی نوتروفیلی (NET) که شامل یک شبکه الیافی متشکل از کروماتین و سرین پروتئاز هستند تشکیل داده که باکتری ها را به دام انداخته و آنها را می کشند.
پژوهش ها نشان میدهند که شبکه خارج سلولی نوتروفیلی کانونهای بسیار متمرکزی از مواد ضد باکتری ایجاد میکنند که با باکتری باند شده و باکتری را به طور مستقل از جذب فاگوسیتوز در غدد پستانی از بین میبرد (Lippolis et al., 2006b; Grinberg et al., 2008). علاوه بر این شبکه خارج سلولی نوتروفیلی می تواند به عنوان یک سد فیزیکی در پیشگیری از گسترش بیشتر باکتری ها در سراسر بافت های گاو به کار گرفته شود.
ایمنی اکتسابی
واکنش ایمنی اکتسابی زمانی آغاز می شود که مکانیسم های ایمنی ذاتی در از بین بردن پاتوژن به شکست انجامد. واکنش سیستم ایمنی اکتسابی با تولید لنفوسیت های ویژه آنتی ژن و سلول های خاطره با توانایی تشخیص عوامل تعیین کننده آنتی ژنیک خاص مشخص می شود.
زمانی که بافت ها و سلول های میزبان مجدداً در معرض آنتی ژن های مشابه قرار می گیرند، وضعیت واکنش ایمنی به صورت حافظه ایمنولوژیکی و تکثیر کلونال سلول های تأثیر گذار آنتی ژن خاص وارد عمل می شوند. پاسخ ایمنی خاطره بسیار سریع تر، به طور قابل ملاحظهای قوی تر، طولانی تر و اغلب مؤثر تر از پاسخ ایمنی اولیه در پاکسازی یک پاتوژن مهاجم خواهد بود. در مقابل پاسخ ایمنی ذاتی، ایمنی اکتسابی می تواند به دلیل تکثیر کلونال لنفوسیت های B و T مخصوص پاتوژن مهاجم چند روز طول بکشد تا توسعه یابد.
یک ویژگی حیرت آور سیستم ایمنی توانایی میزبان در تشخیص و پاسخ به میلیون ها آنتی ژن منحصر به فرد است که ممکن است با آنها مواجه شوند. همچنین مهم است که پاسخ ایمنی غیر معمول علیه آنتی ژنهای میزبان رخ ندهد. به همین دلیل سیستم ایمنی قادر به تشخیص خودی از غیر خودی بوده و به طور انتخابی تنها به آنتی ژن های خارجی واکنش نشان دهد. تنوع ژنتیکی و پروتئین های متصل به غشا که مجموعه سازگاری بافتی اصلی (MHC) نامیده می شوند و مولکول هایی هستند که در این شناخت کمک می کنند. پاسخ ایمنی خاص فقط در صورت ترکیب آنتی ژن با مولکول MHC روی سطح سلولهای معینی رخ می دهد که فرآیندی تحت عنوان پردازش آنتی ژن (antigen presentation) معرفی می شود (Kazansky, 2008). خصوصیات منحصر به فرد پاسخ ایمنی اکتسابی اساس استراتژی واکسن را تشکیل می دهد (جدول 2).
| عامل | عملکردهای اصلی |
| مجموعه سازگاری بافتی اصلی | تشخیص خودی از غیر خودی |
| سلول های دندریتیک و ماکروفاژها | سلول های پردازنده آنتی ژن |
| لنفوسیت های T | سلول های T کمکی (Th1, Th2, Th17, Treg)؛ تولید سیتوکین ها که ایمنی ذاتی و اکتسابی را تنظیم می کنند، تعویض ایزوتایپ های ایمنوگلوبولین سلول های T کشنده (Tc)؛ حمله و از بین بردن سلول هایی که آنتی ژن های خارجی را بیان می کنند (آلوده به ویروس) |
| سلول های γδ T | متداول در نشخوارکنندگان و یافت شده در سطوح موکوسی؛ دفاع ضد میکروبی مهم |
| لنفوسیت های B | سلول های B بالغ سلول های پردازنده آنتی ژن هستند و به سلول های خاطره ویژه آنتی ژن تکثیر می شوند. از سلول های پلاسما ساخته می شوند و آنتی بادی های ویژه آنتی ژن را ترشح می کنند. |
| ایمنوگلوبولین ها (آنتی بادی ها) | IgM بزرگترین و اولین ایمنوگلوبولین تولید شده است؛ نقش در آگلوتیناسیون و فعال سازی سیستم کمکی IgG که غلظت آن در سرم بالاست و برای اپسونین (تحریک به فاگوسیتوز) مهم است. IgA که در سطوح موکوزی یافت می شود و دارای عملکرد آنتی ویروسی است. IgE با واکنش های آلرژیک و عفونت های انگلی در ارتباط است. IgD یک مولکول تنظیم کننده غیر ترشح شده است. |
جدول 2- اجزای سیستم ایمنی اکتسابی
در ایمنی اکتسابی مؤثر دو دسته سلول درگیر می باشند: لمفوسیت ها و سلول های پردازنده آنتی ژن.
لمفوسیتها آنتی ژن های باکتریایی را از طریق گیرنده های غشایی خاص پاتوژن های مهاجم شناسایی می کنند. این ها سلول هایی هستند که در میان ویژگی های تعریف شده ایمنی اکتسابی شامل: اختصاصی، تنوع، خاطره و تشخیص خودی از غیر خودی را دارا می باشند. سلول های B و T زیر مجموعه های متمایزی از لمفوسیت ها هستند که در عملکرد و محصول پروتئین متمایز می باشند. سلول های T می توانند به زیر مجموعه های بیشتر آلفا و بتا (αβ) که شامل CD4+ (T کمک کننده، Th)، CD8+ (T کشنده، Tc) و سلول های T گاما دلتا (γδ) تقسیم شوند. خصوصیت بیشتر سلول های Th به گروه های کار آمد تری نظیر Th1، Th2، Th17 و سلول های T تنظیم کننده (Treg) منجر شده است. بسته به محل بافت، درصد این سلول ها می توانند بسیار متفاوت باشند.
عملکرد سلول های T شامل تولید سیتوکین هایی است که ایمنی سلولی را با تنظیم میزان و مدت پاسخ ایمنی تسهیل می کنند. سلول های Th (نظیر Th1، Th2، Th17 و Treg) سیتوکین هایی را در پاسخ به تشخیص مجموعه سازگاری بافتی اصلی- آنتی ژن روی سلول های پردازنده آنتی ژن (سلول های B، سلول های دندریتیک و ماکروفاژها) تولید می کنند. زمانی که مجموعه سازگاری بافتی اصلی فعال شد، سلول های Th، سیتوکین های متنوعی از تنظیم کننده های سیستم ایمنی را تولید می کنند.
سلول های Th با توانایی تولید سیتوکین های مشخص، نقش مهمی را در فعال سازی سلول های B و T، ماکروفاژها، نوتروفیل ها و دیگر سلول های مختلفی که در پاسخ ایمنی شرکت دارند، بازی می کنند. اختلافات در الگوی ویژه سیتوکین های تولیدی توسط سلول های Th فعال شده، منجر به بروز انواع مختلفی از پاسخ های ایمنی می گردد (Sordillo and Streicher, 2002). سلول های T کشنده، سلول های خودی تغییر یافته را از طریق پردازش آنتی ژن در مولکول های دسته یک MHC ، شناسایی و از بین می برند.
برخی گمانه زنی ها وجود دارد که سلول های T کشنده می توانند به صورت یک لاشه خوار، سلول های ترشحی آسیب دیده و مسن را در غدد پستانی حذف کنند. مشابه سلول های Th، تصور می شود که سلول های T کشنده، پاسخ ایمنی را با رپراتور سیتوکین های تولیدی کنترل و تنظیم می کنند (Aitken et al., 2011). عملکردهای بیولوژیکی سلول های T گاما دلتا، موضوع بسیاری از گمانه زنی ها شده اند. درصد سلول های T گاما دلتا در جمعیت های PBMC گاوی در مقایسه با PBMC انسانی بیشتر است (Baldwin and Telfer, 2015). وظایف این سلول ها در درجه اول محافظت از سطوح اپیتلیال و احتمالاً حد واسط سمیت سلولی با دخالت متغیر MHC می باشد. مولکول های سطحی (WC1) منحصر به فرد موجود در سلول های T گاما دلتا، به صورت گیرنده همراه (Co-receptors) مورد استفاده برای تشخیص پاتوژن های میکروبی و فعال سازی سیگنال دهی سلولی عمل می کنند. این سلولها نقش مهمی را در بیماری های عفونی ایفا می کنند و بنابراین یک خط ویژه دفاعی را در برابر بیماری های باکتریایی ایجاد می کنند (Baldwin and Telfer, 2015).
سلول های B ویژه آنتی ژن با تولید و ترشح آنتی بادی یا ایمنوگلوبولین ها، عوامل ویروسی و میکروبی را شناسایی کرده و با آن مقابله می کنند. سلول های B فعال شده با آنتی ژن که متعاقباً به سلول های پلاسمایی ترشح کننده آنتی بادی تکثیر و تمایز مییابند، ایمنوگلوبولین ها را تولید می کنند. مشخص شده که چند دسته از ایمنوگلوبولین ها دفاع میزبان را در برابر پاتوژن های عفونی تحت تأثیر قرار می دهند که همه آنها در ماهیت فیزیکوشیمیایی و بیولوژیک متفاوت می باشند (جدول 2).
برای مثال چند ایمنوگلوبولین (IgG1 ، IgG2 و IgM) می توانند به شکل اپسونین سبب افزایش فاگوسیتوز توسط نوتروفیل ها و ماکروفاژها شوند. علاوه بر نقش اپسونین، IgM در تثبیت سیستم کمکی کارآمد است. در حالی که، IgA به اپسونین باکتری کمک نمی کند و سبب آگلوتینه شدن باکتری می شود که می تواند مانع توانایی تکثیر پاتوژن های خاص در بافت های معین شود. نقش مهم دیگر IgA توانایی آن در خنثی کردن سموم بعضی از باکتری ها است (Sordillo and Streicher,2002; Aitken et al., 2011). بدیهی است که غلظت و ترکیب ایزوتایپ ایمنوگلوبولین های یافت شده در بافت ها میتواند اثر ژرفی بر ایجاد عفونت های جدید داشته باشد.
اختلالات سیستم ایمنی حول و حوش زایش
دوره انتقال زمانی است که وقوع چند بیماری مهم اقتصادی نظیر؛ ورم پستان، متریت، جابه جایی شیردان و کتوز افزایش می یابد. اختلالات سلامت رخ داده در این دوران به طور خاصی مسئله ساز هستند زیرا به طور قابل توجهی بازده تولید گاو را در شیردهی بعدی تحت تأثیر قرار می دهند. در مدت اوایل شیردهی، بیماری های متابولیکی و عفونی گرایش دارند که در مجموعه ای با یکدیگر رخ دهند و افزایش وقوع هر اختلال در گاو انتقالی، آنها را به دیگر مسائل مربوط به سلامت تسلیم خواهد کرد. برای مثال پژوهش های اپیدمیولوژیک نشان می دهد که یک وابستگی بین گسترش جابه جایی شیردان و وقوع ورم پستان وجود دارد (Emanuelson et al., 1993). علاوه بر این گاوهایی که از کتوز رنج می برند، بیش از دو برابر احتمال درگیر شدن با بیماری ورم پستان دارند (Oltenacu and Ekesbo, 1994). عامل اساسی مسئول در توسعه این اختلالات گاوهای انتقالی، ناکار آمدی سیستم ایمنی میباشد.
تغییرات دینامیکی در بازدهی سیستم ایمنی گاو در زمان زایمان به خوبی مشخص شده است. بررسی های متعددی جنبه های ایمنی ذاتی و اکتسابی مؤثر در حساسیت گاوهای انتقالی به بیماری ها را ارائه کرده اند (Mallard et al., 1998; Aitken et al., 2011; Ingvartsen and Moyes, 2013). نه تنها در گاوهای انتقالی احتمال ابتلا به بیماری بیشتر است بلکه شدت بیماری نیز ممکن است افزایش یابد. واکنش های التهابی ناکارآمد که در سطح سیستمیک و موضعی رخ می دهند، به دلیل اثر مستقیم بر بیماری در گاوهای انتقالی به طور خاصی مسئله ساز است.
اختلالات در پاسخ های التهابی می تواند شامل حالت کاهش پاسخ دهی باشد که با تأخیر مهاجرت کافی نوتروفیل ها و دیگر عوامل سیستم ایمنی ذاتی در مدت اوایل دوره های بیماری مشخص می شود. در واقع بسیاری از پژوهش های پیشین اختلال عملکرد نوتروفیل ها در دوره پیرامون زایش را تشریح کرده اند که شامل؛ اختلال تولید ROS، فعالیت میلوپراکسیداز، کیموتاکسی و فاگوسیتوز (Cai et al., 1994; Kimura et al., 1999; Mehrzad et al., 2001). مشخص شده است گاوهایی که بعداً در اوایل شیردهی درگیر ورم پستان و متریت می شوند، کاهش ظرفیت نوتروفیل در پاسخ به کیموتاکسی و همچنین کاهش ظرفیت تولید ROS در آنها مشاهده می شود (Cai et al., 1994).
در مقابل، فقدان تعادل مناسب بین شروع و اتمام التهاب می تواند منجر به پاسخ مزمن یا بیش از حد قوی التهاب که با آسیب های وسیع بافت های میزبان مشخص می شود همراه باشد. یک نمونه عالی از نتیجه پاسخ التهابی کنترل نشده، شدت و مدت ابتلا به ورم پستان در گاوهای اوایل شیردهی می-باشد. پژوهش ها نشان می دهند که توانایی غدد پستانی در پاسخ دهی سریع به اندوتوکسین E. Coli در اوایل شیردهی نسبت به گاوها در اواسط شیردهی کاهش می یابد (Grommers et al., 1989). مهاجرت تأخیری نوتروفیل ها و کاهش فعالیت ضد میکروبی آنها علت شدت بیشتر ورم پستان کلی فرمی در دوره حول و حوش زایمان نسبت به مراحل بعدی شیردهی می باشد (Hill, 1981; Shuster et al., 1996).
علتهای اساسی اختلال التهاب در طول دوره انتقال موضوع قابل توجه تحقیقات شده است و شواهدی برای حمایت حداقلی از نقش جزئی در تعامل دو طرفه بین سیستم های اندوکرین و سیستم ایمنی وجود دارد.
در واقع پژوهش های انجام شده با استفاده از مدل های برون تنی (in vitro) و درون تنی (in vivo) نشان می دهند که جمعیت های سلول ایمنی نه تنها گیرنده های هورمونی را بیان نمی کنند، بلکه قادر به تولید چندین عامل نورواندوکرین میباشند (Lamote et al., 2006a;Kelley et al., 2007; Weigent, 2013). برای نمونه افزایش چند هورمون استروئیدی در پیرامون زایمان مسئول تغییر عملکرد نوتروفیل ها از طریق تعاملات رسپتور-لیگاند خاص می باشد (Burton et al., 2005). گیرندههای گلیکوکورتیکوئیدی در چند جمعیت سلول ایمنی بیان می شوند و افزایش غلظت گلوکوکورتیکوئید پیرامون زمان زایش عمل قوی سرکوب سیستم ایمنی شناخته می شود (Anderson et al., 1999; Lippolis et al., 2006a; Kelley et al., 2007).
برای مثال، مکانیسمی که توسط گلوکورتیکوئیدها می تواند وظیفه نوتروفیل های خون را دچار مشکل کند شامل؛ کاهش تولید مولکول های چسبنده L-selectin و CD18 مورد نیاز برای فعال سازی مؤثر و مهاجرت به محل بافت آسیب دیده می باشد (Burton et al., 1995). علاوه بر این، گزارش شده تغییر در غلظت های استرادیول و پروژسترون پیش از زایش به طور مستقیم و غیر مستقیم بر قابلیت های عملکردی لمفوسیت ها و نوتروفیلها اثر می گذارد (Roth et al., 1982; Lamote et al., 2006b).
تغییرات در غلظت های پلاسمایی این هورمون های استروئیدی با کل دوره انتقال همپوشانی ندارد و ممکن است دیگر هورمونهای وابسته به دوره انتقال در اختلال ایمنی و التهاب نقش داشته باشند. برای مثال، مشخص شده هورمون های homeorhetic نظیر پرولاکتین، هورمون رشد، IGF و انسولین در طول دوره انتقال به طور قابل توجهی در نوسان بوده و با تغییر متابولیسم و مصرف ماده خشک مرتبط می باشند (Ingvartsen and Andersen, 2000). شواهد زیادی در گونه های انسانی و جوندگان نشان میدهد که پاسخ های ایمنی ذاتی و اکتسابی توسط این هورمون های پروتئینی تحت تأثیر قرار می گیرند (Davis, 1998; Kelley et al., 2007). بنابراین تغییر در بیان هورمون های homeorhetic در پیرامون زمان زایمان و در اوایل شیردهی می تواند عملکرد سلول ایمنی را در گاو انتقالی تغییر دهد.
تغییرات متابولیکی و فیزیولوژیکی مرتبط با زایش و شروع شیردهی در طول دوره انتقال نیز در اختلال پاسخ های ایمنی و التهابی مناسب دخیل است (Sordillo and Raphael, 2013). برای مثال، در یک مجموعهای از پژوهشها، گاوهای شیری آبستن به منظور ارزیابی اثر تولید شیر بر فراسنجه های مختلف ایمنی پستان برداری شدند، این در حالی بود که هنوز هم تغییرات اندوکرینی مرتبط با آبستنی و زایمان حفظ گردید (Kimura et al., 1999, 2002b; Nonnecke et al., 2003).
گاوهای پستان برداری شده نسبت به گاوهایی با غدد پستانی کامل، فقط افزایش اندکی در اسیدهای چرب غیر استرفیه (NEFA) را در طول دوره پیرامون زایمان تجربه کردند. اگر چه عملکرد ایمنی در پیرامون زایش گاوهای پستان برداری شده اندکی به مخاطره افتاد، اما عملکردهای نوتروفیل و لنفوسیت در مدت طولانی تری در گاوهای دارای غدد پستانی کاهش یافت (Kimura et al., 1999; Nonnecke et al., 2003). این محققان اثر منفی شیردهی را بر ترکیب جمعیت های لوکوسیت خون محیطی گزارش کردند (Kimura et al., 2002b).
نتیجه مهم حاصل از این پژوهش ها این است که عمل زایمان ( که با تغییرات در پروفایل هورمون های استروئیدی همراه است) عامل سرکوب سیستم ایمنی در گاوهای حول و حوش زایمان نمی باشد. در عوض، افزایش تقاضای متابولیکی در اوایل شیردهی احتمالاً مسئول اثر منفی بر جمعیت های سلول ایمنی می باشد. تغییرات در مصرف مواد مغذی و در دسترس بودن مواد مغذی ویژه میتواند ارتباط معمول بین اختلال پاسخ های ایمنی و افزایش وقوع بیماری های متابولیکی و عفونی در حول و حوش زایمان گاوهای شیری باشد.
تغذیه و عملکرد ایمنی
مشخص شده است که وضعیت تغذیه ای گاوهای شیری ارتباط نزدیکی با حفظ عملکرد بهینه سیستم ایمنی و سلامت دارد.
احتیاجات تغذیه ای در طول دوره تولید گاوهای شیری متفاوت خواهند بود و هر گونه مدیریت نامناسب احتیاجات غذایی با پاسخ های اختلال عملکرد و اختلالات سلامت مرتبط می باشد. برای مثال پژوهش ها نشان داده اند گاوهای بیش از حد چاق و بیش از حد لاغر وقوع بالاتری از بیماری ها را نسبت به گاوهای با وضعیت بدنی مناسب در اوایل دوره شیردهی دارند (Heuer et al., 1999; Roche et al., 2009). مصرف ماده خشک و تعادل انرژی در زمان خشکی منجر به نمره وضعیت بدنی نامناسب بالا و پایین در دوره زمانی حول و حوش زایمان خواهند شد.
گاوهای لاغر (نمره بدنی کمتر از 3) که از انرژی نا کافی رنج می برند، انرژی و پروتئین مورد نیاز برای ساخت شیر، چربی شیر و مقاومت در برابر بیماریها را از ذخایر بدنی بدست میآورند (Hoedemaker et al., 2009; Roche et al., 2009). در مورد گاوهای چاق (نمره بدنی زایش بیش از 5/3) کاهش طبیعی مصرف ماده خشک بعد از زایمان شدت میگیرد. افت بیشتر DMI در گاوهای چاق منجر به تعادل انرژی منفی شدید (NEB) و تجمع قابل توجه NEFA حاصل از بسیج چربی از ذخایر بافتی می شود. افزایش طولانی مدت NEFA پلاسما در دوران قبل و بعد از زایمان توسط گاو قابل تحمل نبوده و نشان دهنده یک عامل خطر برای اختلالات سلامت گاوهای اوایل شیردهی می باشد (Heuer et al., 1999; Hoedemaker et al.,2009). بنابراین نمره وضعیت بدنی گاوها بایستی قبل و بعد از زایمان به خوبی مدیریت شوند، تا از عواقب نامطلوب بر عملکرد شیردهی و مقاومت بیماری ها جلوگیری شود.
تعادل منفی انرژی و سیستم ایمنی در گاوهای شیری
کاهش DMI و تعادل منفی انرژی عمیقتر در زمان حول و حوش زایمان میتواند از طریق به مخاطره انداختن ظرفیت عملکردی سیستم ایمنی، حساسیت به بیماری را تحت تأثیر قرار دهد.
برای مثال پژوهش های اولیه نشان می دهند که کاهش DMI و افزایش غلظت NEFA به طور موقت با اختلالات عملکرد نوتروفیل خون محیطی در دوره حول و حوش زایمان مرتبط است(Kehrli et al., 1989; Cai et al., 1994). کاهش توانایی عملکردی نوتروفیل در این زمان با اختلالات سلامت در اوایل شیردهی مثل جفت ماندگی و متریت در ارتباط میباشد (Cai et al., 1994; Kimura et al., 2002a; Hammon et al., 2006). علاوه بر این، کاهش عملکرد نوتروفیل میتواند پیش از تشخیص این اختلالات رحم قابل شناسایی باشد (Hammon et al., 2006). مطالعه دیگری در همین ارتباط نشان داد که پاسخ های تکثیر آزمایشگاهی سلول های تک هسته ای خونی محیطی بدست آمده از گاوهای حول و حوش زایمان، پیش بینی کننده بروز بیماری های بعدی بودند.
در این مطالعه، گاوهایی که پاسخ کمتری از سلول های تک هستهای نشان دادند، از ورم پستان کلینیکی، متریت یا درماتیت انگشتی در 60 روز اول شیردهی رنج می بردند (Catalani et al., 2013). شواهد متناقض نشان می دهد که رابطه علت و معلولی اختلال ایمنی حول و حوش زایمان بسیار پیچیده است. مدل های محدودیت غذایی آزمایشگاهی با گاوهای اواسط شیردهی در تلاشی جهت اثر تعادل منفی انرژی مشاهده شده در زمان زایش تکرار شدند. هدف از چنین مدل هایی تعیین اثر کمبود مواد مغذی بر سیستم ایمنی و شدت بیماری بود. با این حال، هیچ یک از این پژوهش ها قادر به تقلید تغییرات گسترده ایمنولوژیکی که در مدت دوره حول و حوش زایمان رخ می دهند، نمی باشد. به عنوان مثال، گاوهایی که در معرض محدودیت تغذیه ای 5 روزه قرار داشتند، تغییرات نسبتاً جزئی را در عملکرد ایمنی پس از چالش ورم پستان نشان دادند (Moyes et al., 2009). دیگر محققان تنها با تعادل منفی انرژی القا شده اثر جزئی روی بیان مولکول های چسبنده لوکوسیت و مولکول های پردازنده آنتی ژن در گاو را گزارش کردند (Perkins et al., 2001).
علاوه بر این، تعادل منفی انرژی القا شده در اواسط شیردهی هیچ اثری روی علائم بالینی ناشی از ورم پستان القا شده از اندوتوکسین حاد را نداشت (Perkins et al., 2002). این اطلاعات به طور کلی نشان می دهد که اگرچه تعادل منفی انرژی و بسیج شدید لیپیدها نقش مهمی را در اختلال ایمنی حول و حوش زایمان ایفا می کنند، اما رفع کمبودهای تغذیه ای و عدم تعادل مواد مغذی و متابولیک رخ داده در زمان زایش، کافی نیست. بیان بازیگرهای کلیدی در محور سوماتوتروپیک می توانند یک عامل کمکی مرتبط با تعادل منفی انرژی باشد و عملکرد سلول ایمنی را با توجه به مراحل مختلف شیردهی تغییر دهد.
در واقع، پژوهش های قبلی نشان داده اند،گاوهای که در تعادل منفی انرژی هستند، تغییرات بیشتری در غلظت هورمون رشد و IGF1 همراه با مقاومت بیشتری نسبت به انسولین دارند که این مورد در گاوهای اوایل شیردهی در مقایسه با گاوهای اواسط شیردهی به مراتب بیشتر است (Gross et al., 2011). با توجه به این واقعیت که جمعیت های سلول های ایمنی دارای گیرنده هایی هستند که می توانند به این هورمون ها پاسخ دهند (Lamote et al., 2006a; Weigent, 2013)، تفاوت ها در سازگاری اندوکرین با تعادل منفی انرژی نسبت به مرحله شیردهی احتمالاً عامل مهمی است که می تواند بر عملکرد سیستم ایمنی بدن تأثیر بگذارد.
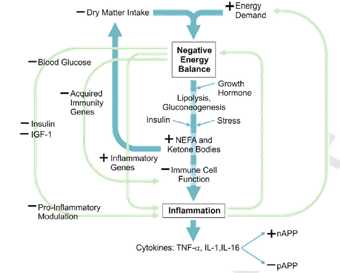
التهاب بعد از زایمان، افزایش متابولیسم سلولی و افزایش بیان ژن ایمنی احتیاجات انرژی را افزایش می دهد در حالیکه DMI پایین است. نمادهای+ و – ، افزایش (+) و کاهش (-) بیومولکول ها را نشان می دهد. NEFA: اسیدهای چرب غیر استریفیه؛ IGF-1: عامل رشد شبه انسولین 1، TNF-α: عامل نکروز کننده α ؛ IL-1 و IL-6 : اینترلوکین 1 و 6؛ nAPP و pAPP: پروتئین های فاز حاد منفی و مثبت.
اسیدهای چرب به عنوان منبع انرژی
اگرچه شواهد موجود حاکی از آن است که تعادل منفی انرژی در حول و حوش زایمان عامل مهمی برای اختلال عملکرد ایمنی است، اما به مکانیسم دقیق این اثرات به طور کامل پی برده نشده است.
به هر حال، افزایش غلظت NEFA پلاسما در مدت بسیج شدید لیپیدها، حداقل نقش جزئی را در تغییر نحوه پاسخ گاوها به چالش های ایمنی در طی دوره انتقال بازی می کند. یک راه مهم که تعادل منفی انرژی شدید و افزایش NEFA پلاسما ممکن است بر مکانیسم های دفاعی میزبان تأثیر بگذارد، تغییر در دسترس پذیری مواد مغذی مورد نیاز برای پاسخ ایمنی مؤثر می باشد. به عنوان مثال در پزشکی در دسترس بودن مقادیر کافی انرژی برای عملکرد های بهینه سیستم ایمنی ضروری است (Calder, 2013). یک سیستم ایمنی فعال نیاز به انرژی قابل توجه و بیشتری نسبت به یک سیستم ایمنی در حال استراحت دارد. در زمان پاسخ التهابی (مثلاً ماکروفاژها و نوتروفیل ها در فاگوسیتوز شرکت خواهند کرد) تولید ROS، بیوسنتز اکسی لیپیدها و ترشح سیتوکین های پیش التهابی همه نیازمند استفاده و بکارگیری انرژی بالایی است (Newsholme et al., 1986). لمفوسیت های تحریک شده با آنتی ژن تحت تکثیر سلولی قرار گرفته و سیتوکین ها و آنتی بادی ها را ترشح می کنند، که یکی دیگی از عملکردهای انرژی گیر سیستم ایمنی محسوب می شوند (Brand, 1985).
بنابراین، سلول های درگیر در پاسخ های ایمنی ذاتی و اکتسابی برای اینکه از یک فنوتیپ ساکن به یک حالت بسیار فعال تبدیل شوند، به انرژی بالایی نیاز دارند. سلول های سیستم ایمنی می توانند سوخت مورد نیازشان را از طریق اسیدهای چرب در دسترس، گلوتامین یا گلوکز با بازده مختلف بدست آورند (Calder, 2013).
توزیع ذخایر انرژی در گاوهای شیری می تواند به طور قابل توجهی در زمان چالش میکروبی تغییر کند، که این خود می تواند تغییرات در بازدهی پاسخ ایمنی را تشریح کند. برای مثال، در پاسخ به ورم پستان کلیفورمی حاد سرعت لیپولیز از ذخایر بافت های چربی به طور معنی داری افزایش می یابد که منجر به افزایش غلظت NEFA پلاسما می شود (Hagiwara et al., 2014; Mavangira et al., 2015). افزایش غلظت NEFA در زمان عفونت می تواند ناشی از کاتابولیسم بافت چربی موجب شده توسط سیتوکین های پیش التهابی نظیر TNFα باشد (Sordillo and Raphael, 2013). افزایش NEFA در پلاسما را می توان به عنوان یک منبع انرژی از طریق فرآیند بتا اکسیداسیون یا به عنوان یک سوبسترا برای تولید گلوکز از طریق گلوکونئوژنز استفاده شود.
گلوکز منبع عمده انرژی برای همه لوکوسیت ها می باشد و در دسترس بودن آن مستقیماً با فعال سازی و عملکرد سلول های ایمنی مرتبط است. فعال سازی لوکوسیت القاء شده میتوژن به برداشت گلوکز و کاتابولیسم آن به منظور فراهم نمودن انرژی مورد نیاز تکثیرشان و فعالیت های ترشحی وابسته است. گلوکز همچنین نقش مهمی را در فعال سازی ماکروفاژها و نوتروفیل ها ایفا می کند. پژوهش های آزمایشگاهی و بالینی انسانی از این مفهوم که غلظت های پایین گلوکز منجر به پاسخ های کمتر از حد مطلوب سیستم ایمنی می شود، حمایت می کند (Calder, 2013). از آنجایی که گلوکز برای عملکرد لوکوسیت ضروری است، اوایل تصور بر این بود که هایپرگلایسمی یک عامل مفید میزبان برای پاسخ به بیماری های حیاتی در انسان محسوب می شود، زیرا گلوکز می تواند سوخت سیستم ایمنی باشد، اما شواهد کنونی نشان می دهد که غلظت بالای گلوکز در خون می تواند پاسخ های التهابی نامطلوب را ایجاد کند.
این به بهترین شکل در بیماران مبتلا به دیابت نوع п ملیتوس نشان داده شده است. این بیماری با مقاومت به انسولین و هایپرگلایسمی مشخص می شود. پاسخ های ایمنی ناکارآمد نظیر؛ کاهش فعالیت های ضد میکروبی نوتروفیل ها و ماکروفاژها باعث اختلال در تعاملات پاتوژن –میزبان در زمان دیابت می شود که بخشی از آن ناشی از تغییر متابولیسم گلوکز است. وضعیت هایپرگلایسمی همچنین می تواند فعال سازی لوکوسیت های را افزایش داده و منجر به واکنش التهابی غیر قابل کنترل و شدید شود که در بیماران مبتلا به دیابت به بیماری زایی عامل بیماری کمک می کند (Calder et al., 2007; Hodgson et al., 2015). به طور خلاصه، اکنون در علم پزشکی هایپوگلایسمی و هایپرگلایسمی می توانند بر سیستم ایمنی میزبان و حساسیت به بیماری ها تأثیر گذار باشند (Calder et al., 2007).
براساس آنچه در سایر گونه ها شناخته شد، توزیع و استفاده از ذخایر انرژی می تواند به طور قابل توجهی بر نحوه پاسخ گاوهای شیری به هر نوع چالش ایمنی پاسخ دهد. در واقع، نیاز متابولیکی دوره حول و حوش زایش منجر به تغییرات چشمگیر در مصرف و توزیع گلوکز می شود، به طوری که عمده گلوکز در دسترس جهت سنتز و ترشح شیر اختصاص می یابد. تا به امروز هیچ مطالعه ای مستقیماً نحوه رقابت سلول های سیستم ایمنی را برای گلوکز موجود در زمان شروع سنتز و ترشح شیر مورد بررسی قرار نداده است. در هر صورت، گام محدود کننده برای برداشت و استفاده از گلوکز توسط سلول های میزبان با بیان گروهی از انتقال دهنده ها (GLUT) در سطح سلول تعیین می شود(Calder, 2013).
پژوهش های اخیر نشان می دهند که بیان GLUTs توسط سلول های ایمنی گاوی در اوایل شیردهی به طور قابل توجهی کاهش می یابند (O’Boyle et al., 2012). این یافته ها از این مفهوم حمایت می کند که سلول های سیستم ایمنی می توانند در مقایسه با آنچه برای تولید شیر استفاده می شود کمتر برای گلوکز رقابت کنند، بنابراین پدیده اختلال سیستم ایمنی در دوره حول و حوش زایمان تشریح می شود. به محض تحریک اندوتوکسین، بیان GLUT بر روی مونوسیت ها افزایش می یابد و با تولید TNFα رابطه مثبت دارد که این امر را تأیید می کند که جذب گلوکز برای عملکردهای پیش التهابی ضروری است (O’Boyle et al., 2012). در واقع ضرورت فوری بقا پس از حمله پاتوژن می تواند منجر به اختصاص گلوکز به سیستم ایمنی شود به جای پاسخ های فیزیولوژیک غیر ضروری مثل تولیدمثل و شیردهی. بنابراین سیستم ایمنی فعال شده می تواند مواد مغذی محدود را از دیگر فرآیندهای مربوط به تولید منحرف کند و یک توضیح احتمالی برای کاهش تولید گاوهای شیری مبتلا به اختلالات سلامتی ارائه دهد.
اسیدهای چرب و سیگنال دهی داخل سلولی
اگرچه افزایش NEFA پلاسما می تواند به طور غیر مستقیم از طریق ظرفیت آن به عنوان یک منبع انرژی سیستم ایمنی را تحت تأثیر قرار دهد، شواهد فراوانی نشان می دهند که اسیدهای چرب می توانند عملکرد سلول های ایمنی را مستقیماً تغییر دهند.
تغییر در ترکیب اسیدهای چرب جمعیت های سلول ایمنی مسئول تأثیر بسیاری از جنبه های پاسخ های ایمنی ذاتی و اکتسابی به چند روش مختلف است. برای مثال نوع اسیدهای چرب موجود در غشاء فسفولیپیدی می تواند سیالیت غشا و عملکرد سلول های ایمنی را از طریق شکل دهی به گستره چربی (lipid raft) تحت تأثیر قرار دهد (Raphael and Sordillo, 2013). گستره غشا میکرودومین های گلیکوپروتئینی تخصصی هستند که رفت و آمد پروتئین غشا و گیرنده باند کننده سلولی مانند آنچه که در فعال سازی لمفوسیت ها، تولید آنتی بادی و التهاب درگیر است را تحت تأثیر قرار می دهند.
برای مثال ترکیب و یکپارچگی گستره های چربی برای فعال سازی CD14 ضروری است زیرا داروهای مخرب گستره ها می توانند LPS القاء کننده تولید TNF نظیر آنچه که در عفونت باکتری های گرم منفی تولید می شوند را بلوکه کنند (Luo et al., 2008). فسفولیپیدهای غشای لوکوسیت گاوهای شیری حاوی سهم های قابل توجهی از اسیدهای پالمیتیک و استئاریک می باشد (Contreras et al., 2010). محتوای بالای اسیدهای چرب اشباع می تواند به شکل کووالانسی پروتئین ها را از طریق آسیلاسیون تغییر دهد و نه تنها بر نحوه اتصال پروتئین ها به غشا اثر گذاشته که خود سیالیت غشا را تغییر می دهد، بلکه شکل گیری گستره چربی ها و بنابراین عملکرد سلولی مؤثر است (Raphael and Sordillo, 2013).
علاوه بر تغییر ماهیت فیزیکی غشاهای سلولی، انواع مختلف اسیدهای چرب قادر به تنظیم مسیرهای سیگنال دهی داخل سلولی و فعال سازی عامل رونویسی بوده و می توانند منجر به تغییر بیان ژن شوند. برای مثال، عامل رونویسی التهابی NFκB زمانی فعال می شود که گیرنده های تشخیص پاتوژن TLR4 روی سلول های میزبان با LPS متصل به غشای خارجی باکتری های گرم منفی ارتباط برقرار کنند (Kawai and Akira, 2011). مشخص شده که اسیدهای چرب غیر اشباع مشخصی نظیر EPA و DHA دارای عملکردهای ضد التهابی با مهار فعال سازی NFκB القا شده LPS از طریق یک مکانیسم واسط TLR4 می باشد (Lee et al., 2010).
EPA و DHA می توانند عملکردهای ضد التهابی روی مولکول های سیگنال دهنده NFκB را به طور غیر مستقیم از طریق اثر متقابلشان با دیگر مسیرهای سیگنال دهنده شامل گیرنده فعال کننده تکثیر پراکسی زوم ها و عوامل رونویسی (SREBPs) اعمال کنند (Clarke, 2004). در عوض، نشان داده شده است که چند اسید چرب اشباع نظیر لوریک، میریستیک و پالمیتیک اسید، ژن واسط NFκB را از طریق سیگنال وابسته به TLR4 بیان می کنند هر چند تردید وجود دارد که آیا این عمل روی باند کردن TLR4 مستقیم است یا غیر مستقیم (Erridge and Samani, 2009; Lee et al., 2010). با این وجود، صرف نظر از اثر کلی اسیدهای چرب اشباع یا غیر اشباع روی NFκB القا کننده التهاب به نظر می رسد که تغییر چندین ژن مرکزی برای پاسخ التهابی شامل COX2، TNF-α و IL1 باشد (Lee et al., 2010).
اسیدهای چرب به عنوان سوبستراهای اکسی لیپیدها
یکی از راه هایی که ترکیب اسیدهای چرب سلول می تواند پاسخ های ایمنی را تحت تأثیر قرار دهد، تنظیم کردن تولید واسط های قوی لیپیدی یا اکسی لیپیدهایی هستند که اساساً هر جنبه ای از آغاز و حل پاسخ های التهابی را تنظیم می کنند.
همانطور که در بخش های قبلی بحث شد، اکسی لیپیدها عمدتاً از اسیدهای چرب غیر اشباع n-6 (اسیدهای لینولئیک و آراشیدونیک اسید) یا n-3 (EPA و DHA) موجود در فسفولیپیدهای غشای سلولی و از طریق مسیرهای مختلف اکسیداسیون و احیا ساخته می شوند (Raphael and Sordillo, 2013). از نظر تاریخی، تصور می شود که اکسی لیپیدها مشتق شده از اسیدهای چرب غیر اشباع n-6 (مثل PG، LT و TX) در واکنش های پیش التهابی شرکت دارند در حالی که اکسی لیپیدهای بیوسنتز شده از اسیدهای چرب غیر اشباع n-3 غالباً موجب کاهش التهاب می شوند (Serhan et al., 2008). با پیشرفت در توانایی های تحلیلی، در حال حاضر به طور گسترده ای مشخص شده است که این فرضیات اولیه بیش از حد ساده بوده و شبکه اکسی لیپیدها پیچیده، بسیار تعاملی و اغلب ویژه سلول در سازماندهی شروع یا پایان پاسخ های التهابی است (Arnardottir et al., 2015; Mavangira et al., 2015; Ryman et al., 2015b).
پروفایل بیوسنتزی اکسی لیپیدها و اثر متعاقبی که ممکن است این متابولیت ها بر پاسخ التهابی داشته باشند نه تنها به در دسترس بودن سوبستراهای PUFA مختلف، بلکه به زمان متابولیسم بعدی آنها از طریق مسیرهای مختلف اکسید شدن نیز بستگی دارد. به عنوان مثال آراشیدونیک اسید متابولیزه شده از طریق مسیر COX، اکسی لیپیدهایی با عملکرد مخالف روی سفتی عروق تولید خواهد کرد. پروستاسیکلین (PGI2) سبب گشاد کردن عروق و مانع تجمع پلاکت ها می شوند، در حالیکه ترومبوکسان A2 (TXA2) باعث تجمع پلاکت ها و انقباظ عروق می شود. از آنجاییکه PGI2 و TXA2 از حد واسط مشابه محصول COX (PGG2) مشتق شده است، بیان متعادل این اکسی لیپیدها از طریق مسیرهای آنزیمی پایین دستی مختلف برای سلامت بهینه عروق و توانایی های سیستم ایمنی بسیار مهم است (Ryman et al., 2015a).
در واقع، پژوهش های قبلی با استفاده از سلول های اپیتلیال گاوی نشان داد که تنش اکسیداتیو می تواند سنتز پروستاسیکلین و شکل گیری PGI2 مهار کند و در نتیجه باعث اختلال در هموستازی عروق شود (Weaver et al., 2001). علاوه بر این، فرضیات پیشین مبنی بر اینکه همه متابولیت های COX2 و 15LOX به تنهایی مسئول انتشار پاسخ التهابی هستند با منابع علمی کنونی حمایت نمی شوند.
برای مثال PGE2 مشتق شده از آراشیدونیک اسید که از مسیرCOX2 بدست آمده است، به عنوان عامل داشتن فعالیت های پیش التهابی متعدد مثل القای درد و تب شناخته شده است. در حالیکه افزایش بیان COX2 در زمان شروع التهاب با تولید PGE2 مشخص می شود و افزایش بیان COX2 در طول پایان التهاب به حضور متابولیت های COX2 مشتق شده از آراشیدونیک، PGD2 و 15d-PGJ2 مربوط می شود. PGD2 و هم محصول نهایی دهیدراسیون آن 15d-PGJ2، می توانند چسبیدن لوکوسیت ها به سلول های اندوتلیال را مهار کرده و بیان سیتوکین را با بلوکه کردن فعال سازی NFκB کاهش دهند (Pattanaik and Prasad, 1998).
شواهد نشان می دهد که PGE2 می تواند نقش مهمی را در راه اندازی پایان التهاب با افزایش فعالیت LOX و درنتیجه تشکیل لیپوکسین A4 مشتق شده از آراشیدونیک با ماهیت ضد التهابی قوی، ایفا کنند (Serhan and Chiang, 2008). لیپوکسین ها با فرآیند بیوسنتز بین سلولی شامل اعمال ترتیبی LOX از حداقل دو نوع سلول مختلف تولید می شوند.
برای مثال اکسیداسیون اولیه اسید آراشیدونیک از طریق مسیر 15LOX در سلول های اپیتلیال انسان یک پیش ساز 15HETE (15-هیدروکسی ایکوزا تترانوئیک اسید) تولید می کند که سپس از طریق مسیر 5LOX در ماکروفاژها برای تولید LXA4 و LXB4 متابولیزه می شود. در مقابل، متابولیسم آراشیدونیک توسط 5LOX در لوکوسیت ها و تولید LTA4 می تواند توسط 15LOX در پلاکت ها برای بیوسنتز LX به کار رود (Serhan et al., 2008). تغییرات زمان و نسبت بیوسنتز اکسی لیپیدها از طریق مسیرهای LOX در سلامت گاوهای شیری قابل توجه است.
به عنوان مثال یک عدم تعادل در نسبت LXA4 به LTB4 در زمان ورم پستان رخ می دهد و به علت کاهش چشمگیر بیوسنتز LXA4 در داخل غدد پستان آلوده گزارش شده است (Boutet et al., 2003). اخیراً استفاده از کروﻣﺎﺗﻮﮔﺮاﻓﻰ ﻣﺎﯾﻊ – ﻃﯿﻒ ﺳﻨﺠﻰ جرمی یک روش قوی تری را برای شناسایی شبکه اکسی لیپید گسترش یافته در زمان ورم پستان ارائه می دهد. یافته های اصلی حاصل از مطالعه این بود که اکسی لیپیدهای ساخته شده از طریق مسیرهای LOX و سیتوکروم P450 ، فراوان ترین واسط های لیپیدی تولید شده در زمان ورم پستان کلیفرمی حاد می باشد (Mavangira et al., 2015). با در نظر گرفتن تکنیک های تحلیلی پیشرفته در دسترس، مشخص شده است که بیوسنتز اکسی لیپید در زمان ورم پستان بسیار پیچیده است و به در دسترس بودن PUFA، فعالیت مسیرهای بیوسنتتیک و درجه ای که هر محصول اکسید شده بیشتر در غدد پستانی متابولیزه می شود، بستگی دارد.
امکان استفاده از استراتژی های مداخله گرایانه غذایی به منظور اصلاح و بهبود در دسترس قرار دادن سوبسترا برای بیوسنتز اکسی لیپیدها در طول سلامت و بیماری، برخی اهداف تحقیق را به خود اختصاص داده است. برای مثال، تغذیه مکمل PUFA n-3 تولید PGF2α را کاهش داده و سلامت رحم را در گاوهای اوایل شیردهی بهبود می دهند (Mattos et al., 2004; Dirandeh et al., 2013). زمانی که اسیدهای چرب n-3 در جیره مکمل می شوند، ماهیت عملکردی لنفوسیت ها و سلول های تک هسته ای گاوهای دوره انتقال تعدیل می شود (Lessard et al., 2004).
علاوه بر این، آزمایش بزرگی انجام شد که در آن جیره گاوها پیش از زایمان به منظور کاهش نسبت اسیدهای چرب n-6 به n-3 تعدیل شد. محققان گزارش کردند، که با مکمل کردن اسیدهای چرب n-6 ایمنی ذاتی بهبود یافت به طوریکه با پاسخ های فاز حاد بهتر و ارتقاء عملکرد نوتروفیل ها در دوره انتقال نشان داده شد (Silvestre et al., 2011).
| ماده مغذی | جزء فعال | عملکرد |
| ویتامین A | بتاکاروتن | ممانعت از واکنش های زنجیری پر اکسیداسیون |
| ویتامین C | آسکوربیک اسید | از بین برنده رادیکال ها |
| ویتامین E | آلفا توکوفرول | مختل کننده واکنش زنجیری پر اکسیداسیون اسیدهای چرب |
| سلنیوم | تیوردوکسین ردکتاز | سیگنال دادن اکسیداسیون-احیا و کاهش گونه های اکسیژن فعال (ROS) |
| سلنیوم | گلوتاتیون پراکسیداز | سیگنال دادن اکسیداسیون-احیا و کاهش ROS |
| مس | سرولوپلاسمین | فعالیت اکسیداز، از بین برنده رادیکال پروکسیل |
| مس-روی | سوپراکسید دیسموتاز | تبدیل سوپر اکسید سیتوزول به H2O2 |
| روی | متالوتیونین | از بین برنده رادیکال غنی از سیستئین |
| منگنز | سوپر اکسید دیسموتاز | تبدیل میتوکندریایی سوپر اکسید سوپر اکسید به H2O2 |
| آهن | کاتالاز | تبدیل H2O2 به آب |
جدول 3 – مکانیسم های آنتی اکسیدان فراهم شده توسط ریز مغذی ها
اثر مستقیم افزایش محتوای PUFA ، n-3 سلول های ایمنی نیز ارزیابی شد. استفاده از سلول های اندوتلیال کشت شده و پژوهش های قبلی نشان داد که پاسخ های پیش التهابی، در واکنش به غلظت بالای NEFA به تقلید از بسیج شدید چربی ها در گاوهای دوره انتقال، کاهش می یابد (Contreras et al., 2012a,b). این پژوهش های درون آزمایشگاهی اولین شواهد مستقیم را ارائه دادند که کاهش پاسخ های التهابی می تواند ناشی از تغییرات در پروفایل اکسی لیپیدها در پی مکمل n-3 باشد، نظر به اینکه تغییرات قابل توجهی در بیان اکسی لیپیدهای از بین برنده التهاب نظیر resolvin، protectin و lipoxin وجود دارند (Contreras et al., 2012a).
در مجموع منابع کنونی این مفهوم را تأیید می کنند که مکمل کردن جیره گاوها با PUFA می تواند بیوسنتز اکسی لیپید را تحت تأثیر قرار دهد و ظرفیت عملکردی سلول های درگیر در ایمنی و پاسخ های التهابی را به طور مؤثری تغییر دهد.
ریز مغذی ها، تنش اکسیداتیو و ایمنی
به طور گسترده ای مشخص شده است که ریزمغذی های جیره غذایی (ویتامین ها و عناصر معدنی کم مصرف) در صنعت گاو شیری، در تضمین بازده تولید و توانمندی سیستم ایمنی در اوایل دوره شیردهی نقش مهمی دارند (جدول 3). در واقع، کمبود ویتامین ها و عناصر کم مصرف در طول زمان حول و حوش زایمان با افزایش وقوع چند بیماری نظیر ورم پستان، جفت ماندگی و متریت همراه است (Zhao et al., 2015). ریز مغذی های مختلف که از عملکردهای سیستم ایمنی حمایت می کنند و بر وقوع اختلالات سلامت تأثیر گذارند در چندین مقاله مروری جامع متمرکز شده است (Wilde, 2006; Andrieu, 2008;Spears and Weiss, 2008; Sordillo and Aitken, 2009) و در جزئیات در این مقاله پوشش داده نخواهند شد. در عوض، این مقاله به بررسی مکانیسم زیر بنایی متداولی خواهد پرداخت که توسط آن اکثر ریز مغذی ها بر ظرفیت عملکردی جمعیت سلول های ایمنی و وقوع و شدت بیماری تأثیر می گذارند.
یکی از مکانیسم های متداولی که توسط آن اکثر ریز مغذی ها، زمینه را برای بهینه سازی سیستم ایمنی فراهم می کنند، از طریق توانایی های آنتی اکسیدانی می باشد. آنتی اکسیدان ها می توانند به طور گسترده ای به ماده ای تعریف شوند که آسیب اکسیداتیو را برای هدف قرار دادن ماکرومولکول تأخیر انداخته، ممانعت کرده و یا حذف نمایند (Valko et al., 2007; Sordillo and Aitken, 2009). از بین رفتن هموستازی اکسیداسیون-احیاء (Redox) و آسیب به بافت ها، حاصل از تجمع بیش از حد ROS یا کاهش دفاع های آنتی اکسیدانی تحت عنوان تنش اکسیداتیو شناخته می شوند.
پژوهش های قبلی نشان داده اند که تنش های اکسیداتیو عامل مهمی است که می تواند در بروز پاسخ های التهابی غیر طبیعی در گاوهای تحت تنش متابولیکی در دوره انتقال به علت عدم توازن در بیان ROS و در دسترس پذیری عوامل آنتی اکسیدانی، شرکت کند (Sordillo and Aitken, 2009). منبع ROS در گاوهای انتقالی ناشی از تبدیل مواد مغذی به منبع انرژی مورد نیاز برای تأمین سوخت جهت سنتز و ترشح شیر می باشد که از طریق یک سری واکنش های متابولیکی که مجموعاً تنفس سلولی نامیده می شود، رخ می دهد. گونه های فعال اکسیژن متابولیت هایی هستند که در میتوکندری به عنوان محصولات فرعی زنجیره انتقال الکترون تشکیل می شوند (Valko et al., 2007). در گاوهای شیری، منبع مهم ROS در دوره انتقال، بتا اکسیداسیون پراکسی زومی در کبد در زمان متابولیسم اسیدهای چرب می باشد (Drackley, 1999; Grum et al., 2002). اکثر ROS های موجود در بافت های سالم احتمالاً از افزایش متابولیسم سلولی و تولید انرژی توسط میتوکندری حاصل می شوند.
با این حال منابع بالقوه دیگری از ROS عبارتند از؛ مسیرهای آنزیمی اکسید کننده مختلف مرتبط با پاسخ التهابی می باشد. به عنوان مثال؛ سیستم NADPH اکسیداز یافت شده در سلول های ایمنی فاگوسیت کننده مقادیر قابل توجهی ROS در زمان انفجار تنفسی تولید می کنند که پاتوژن های میکروبی را از پای در می آورد (Babior, 1999). بیوسنتز اکسی لیپیدها در زمان پاسخ التهابی نیز می تواند به طور قابل توجهی ROS تولید کند. فسفو لیپیدهای غشایی می توانند از طریق مسیرهای LOX، COX و یا سیتوکروم P450 تحت اکسیداسیون آنزیمی قرار گیرند که نه تنها منجر به ایجاد هیدروپر اکسید لیپیدی بسیار فعال می شود بلکه آنیون سوپر اکسید به عنوان یک محصول فرعی واکنش نیز تولید می شود (Raphael and Sordillo,2013).
تولید بعضی ROS ها از این منابع مختلف برای تنظیم فرآیندهای سلولی نظیر کنترل ایمنی و پاسخ های التهابی ضروری است. برای مثال شواهد نشان می دهند که ROS به عنوان پیامبر در انواع مسیرهای سیگنال دهی تنظیم اکسیداسیون-احیا مانند NFκB و مسیر پروتئین کیناز فعال کننده میتوژن به کار گرفته می شوند که منجر به تولید سیتوکین ها، اکسی لیپیدها و دیگر عوامل ضروری تنظیم کننده سیستم ایمنی برای پاسخ های التهابی و بهینه ایمنی می شود (Finkel, 2011; Brown and Griendling, 2015). بنابراین، مقادیر کم تا متوسط ROS می توانند برای سلامت گاوهای شیری در زمان مواجه شدن با چالش میکروبی یا دیگر منابع آسیب بافتی مفید باشند.
با این حال، مشکلات سلامت زمانی رخ می دهند که دفاع آنتی اکسیدانی ناکافی بوده و تجمع ROS افزایش می یابد، که موجب آسیب به ماکرومولکول های بافتی نظیر DNA، پروتئین ها و لیپیدها می شود. به عنوان مثال، رادیکال های هیدروکسیل در انسان می توانند باعث ایجاد شکست هایی در رشته های DNA، تغییرات بازهای پورینی و پریمیدینی و تغییرات در مولکول های قند دئوکسی ریبوز مرتبط با سرطان و پیری شوند (Valko et al., 2007). اهداف اصلی آسیب ROS لیپیدها هستند و در گاو شیری شواهدی وجود دارد که در طول دوره انتقال، پر اکسیداسیون بیش از حد لیپید رخ می دهد (Bernabucci et al., 2005; Sordillo et al., 2007; Sordillo and Aitken, 2009). پر اکسیداسیون لیپیدی شامل یک فرآیند واکنش زنجیری است که در زمان حضور ROS آغاز می شود مانند رادیکال های هیدروکسیل که الکترون ها را از لیپیدها در غشاهای سلولی به دست می آورند.
انتزاع الکترون ها از اسیدهای چرب منجر به تولید رادیکال پر اکسید لیپیدی می شود که سبب یک واکنش زنجیری خود به خودی در غشاء پلاسمایی شده و الکترون های اضافی از اسیدهای چرب مجاور حذف می شوند. محصولات پر اکسیداسیون لیپیدی می توانند به غشاء سلول و اندامک هایی که در تغییر عملکرد سلولی و انتقال سیگنال نقش دارند، آسیب برسانند.
پژوهش های کنترل شده با استفاده از سلول های اندوتلیال گاوی شواهد مستقیمی را فراهم می کند که شرایط تنش اکسیداتیو تولید هیدرو پراکسیدهای لیپیدی را افزایش خواهد داد و پاسخ های التهابی و اختلالات عملکرد اندوتلیوم عروقی را تشدید می کنند (Sordillo et al., 2005, 2008). بنابراین برای بافت های میزبان مهم است که دارای ظرفیتی باشند تا تجمع ROS ها را به مقدار غیر سمی به منظور عملکرد بهینه سلول ایمنی تنظیم نمایند (Sordillo et al., 2005, 2008).
مکانیسم های آنتی اکسیدانی شامل شبکه پیچیده ای از عواملی هستند که ظرفیت غیر فعال کردن ROS های مضر تولید شده (حاصل از فعالیت های طبیعی سلولی و در زمان فعالسازی سلول ایمنی تا هجوم پاتوژن ها) را دارا می باشند. چند ویتامین و عنصر کم مصرف اجزای ضروری سیستم دفاعی آنتی اکسیدانی هستند، و کمبود هر یک از آنها سیستم ایمنی را به مخاطره انداخته و حساسیت به بیماری ها را در گاوهای شیری افزایش می دهد (Spears and Weiss, 2008). به طور کلی، عملکرد آنتی اکسیدانی ویتامین ها و مواد معدنی را می توان با داشتن ظرفیت فرونشاندن اکسیدان ها به طور مستقیم یا تشکیل بخشی از زوج های آنزیمی اکسیداسیون-احیایی که ROS را به متابولیت های کمتر واکنش پذیر تبدیل می کنند، شناخت (جدول 3).
برخی نمونه های از بین برنده رادیکال ها به ریز مغذی ها نظیر توکوفرول ها، اسکوربیک اسید، کارتینوئیدها و گلوتاتیون ارتباط داشته یا از چنین ترکیباتی مشتق می شوند. سیستم های آنزیمی مهم از بین برنده ROS نیز به ریز مغذی ها وابسته اند که شامل کاتالاز، سوپراکسیددیسموتاز و سیستم های آنزیمی وابسته به سلنیوم می باشد (Sordillo and Aitken, 2009). بین پژوهش های گسترده مکانیسم های دفاع آنتی اکسیدانی در گاوهای شیری، سیستم های آنزیمی وابسته به سلنیوم نظیر گلوتاتیون پراکسیداز سیتوزول (GPX1) و تیوردوکسین ردوکتاز (TRX1) در جایگاه فعال خود دارای ریشه های سلنوسیستئین می باشند.
GPX1 و TRX1 با احیای H2O2 و هیدروپراکسیدهای اسیدهای چرب به ترتیب به آب و الکل واکنش پذیری آنها را کاهش می دهند. برای مثال GPX1 می تواند طیف وسیعی از هیدروپراکسیدها را با مصرف زوج اکسایشی-کاهشی آن و گلوتاتیون احیا کند. به طور متناوب، گروه های سیستئین اکسید شده روی پروتئین ها می توانند با استفاده از مرکز فعال اکسایش-کاهش تیوردوکسین به شکل پیوندهای دی سولفید که خود توسط TRX1 و NADPH احیا می شوند، احیا گردند (Sordillo and Aitken, 2009). دیگر سیستم های آنزیمی که نقش مهمی در جلوگیری از تشکیل رادیکال های اکسیژن ایفا می کند شامل کاتالاز حاوی آهن، سوپر اکسید دیسموتاز سیتوزولی (مس و روی) و سوپر اکسید دیسموتاز میتوکندریایی (منگنز و روی).
آنتی اکسیدان ها همچنین به عنوان از بین برنده رادیکال آزاد عمل می کنند زمانی که آنها با دادن یک الکترون به ROS، آن را پایدار کرده و به این ترتیب به یک رادیکال اکسید شده اما پایدار تبدیل می شوند. برای مثال آلفا توکوفرول (ویتامین E)، رادیکال های پر اکسید لیپید را با اهدای یون هیدروژن از بین برده و سپس به یک رادیکال توکوفرول تبدیل می شود. رادیکال توکوفرول می تواند به شکل احیا شده آن توسط اسید اسکوربیک (ویتامین C) احیا شود. بدین ترتیب، اسید اسکوربیک نقش مهمی را در حفظ وضعیت اکسیداسیون-احیاء سلول ها علاوه بر نقش از بین برندگی رادیکال های آزاد برای دیگر بیومولکول های اکسید شده دارد (Sordillo and Aitken, 2009).
پیش ساز ویتامین A، بتاکاروتن یکی دیگر از مهم ترین از بین برنده های رادیکال های آزاد است. کارتینوئیدها به طور مؤثری اکسیژن واحد را رفع کرده و می توانند از تشکیل ROS ثانویه جلوگیری کنند. اگرچه ریز مغذی ها اجزای ضروری شبکه دفاع آنتی اکسیدانی هستند، توجه به این نکته مهم است که غلظت های پلاسمایی ویتامین ها و مواد معدنی در گاوهای شیری در زمان پیرامون زایمان کاهش می یابد. کاهش دسترسی به ریزمغذی های موجود در سرم احتمالاً به دلیل ترکیبی از کاهش مصرف خوراک و همچنین افزایش میزان استفاده از آنها در تنش های متابولیک گاوهای انتقالی می باشند (Spears and Weiss, 2008; Sordillo and Mavangira, 2014). غلظت ویتامین ها و مواد معدنی در جیره گاوهای شیری، نباید بر اساس آنچه که برای به حداکثر رساندن بهره وری تولید نیاز است، مکمل شوند، بلکه لازم است بر اساس سیستم ایمنی پایه ریزی شود که از تنش اکسیداتیو جلوگیری کرده و عملکرد سلول ایمنی را بهینه کند.
سنجش وضعیت و عملکرد سیستم ایمنی
توسعه استراتژی های مؤثر تغذیه ای به منظور بهینه سازی ایمنی گاو شیری نیازمند روش های قابل اعتماد و دقیق برای اندازه گیری قابلیت های ایمنی بدن است.
به دلیل پیچیدگی سیستم ایمنی، روش های مختلفی برای ارزیابی پاسخ های سیستم ایمنی ذاتی و اکتسابی وجود دارد. برای ارزیابی وضعیت ایمنی گاوهای شیری در پاسخ به استراتژی های تغذیه ای، می توان از چند روش کلی استفاده کرد. روش اول، خون، خط لوله سیستم ایمنی است و ساده ترین روش برای ارزیابی پروفایل سلولی و اجزاء محلول ایمنی در خون است. اگرچه برای منبع عفونت، دامنه های طبیعی و ارزیابی شده شمار لوکوسیت خون و غلظت پروتئین های فاز حاد خون به خوبی مشخص نشده اند، اما تعیین تغییرات در فراسنجه های خون معمولاً در دامپزشکی به منظور ارزیابی وضعیت ایمنی مورد استفاده قرار می گیرد.
یکی دیگر از روش های رایج برای ارزیابی عملکرد ایمنی گاو شیری جداسازی سلول های ایمنی از خون و بررسی فعالیت آنها در آزمایشگاه می باشد. روش های آزمایشگاهی مختلفی برای تعیین قابلیت های ایمنی ذاتی و اکتسابی در دسترس می باشند. روش های ارزیابی ظرفیت ایمنی را می توان با اندازه گیری ظرفیت عملکرد سلول های ایمنی جدا سازی شده معطوف داشت. با ارزیابی فنوتیپی خون و جمعیت لوکوسیت های موضعی با استفاده از جریان سیتومتری می توان به درک بالاتری نسبت به ظرفیت ایمنی دست یافت. با این حال، مستقیم ترین روش ارزیابی وضعیت ایمنی، مطالعه نحوه پاسخ گاوها در شرایط مزرعه ای به چالش ایمنی است.
واکسیناسیون یک روش چالش ایمنی است که می تواند با اندازه گیری آنتی بادی های خاص آنتی ژن ارزیابی شود. یکی دیگر از روش های مستقیم، ارزیابی الگوی حساسیت به بیماری یا درجه پاتوژنز مربوط به ظرفیت عملکرد تغییر یافته واکنش های خاص ایمنی خواهد بود. حوزه مهیج و نسبتاً جدید برای ارزیابی تغییرات در وضعیت ایمنی گاو شیری در زمان سلامت و بیماری شامل استفاده از ابزارهای تشخیص سلولی و مولکولی پر بازده است. در دهه اخیر استفاده از متدولوژی ژنومیک، پروتئومیک و متابولومیک، درک ما را در مورد واکنش های مهم ایمنی در چند مدل بیماری که در صنعت گاو شیری دارای اهمیت اقتصادی هستند دچار تغییر کرده است (Sordillo and Mullarky, 2010; Boggess et al., 2013; Thompson-Crispi et al., 2014).
همچنان که بسیاری از روش ها در ارزیابی پاسخ های ایمنی به مداخلات تغذیه ای وجود دارند، تشخیص بهترین شاخص های وضعیت ایمنی با چند عامل مشکل است. تفسیر مناسب هر ارزیابی ایمنی باید بر اساس مقادیر بحرانی برای دامنه های طبیعی و غیر طبیعی باشد. متأسفانه، بسیاری از عوامل فیزیکی و محیطی می توانند ایمنی را تحت تأثیر قرار داده و چنین محدوده هایی در حال حاضر در دسترس نیستند. همچنین تنوع قابل توجه در تک تک حیوانات با ارزیابی ایمنی خاص، حتی زمانی که یک گله ارزیابی می شود، وجود دارد.
نهایتاً، بسیاری از روش های ارزیابی عملکرد ایمنی در آزمایشگاه های مختلف انجام می شوند که مقادیر بین مطالعات را به منظور ارزیابی مقادیر مطلق مقایسه می کنند. چنانکه، مشخص شده است که پاسخ های ایمنی در گاوهای شیری، برای بهینه سازی مقاومت به بیماری حیاتی هستند، چنین پاسخی می تواند یک روش استاندارد و یکنواخت که پیش بینی کننده دقیق وضعیت ایمنی باشد، فراهم کند.
نتیجه گیری
اگرچه ارتباط سببی مستقیم در گاو وجود ندارد، اما شواهد متعدد نشان می دهد که افزایش بیماری های متابولیک و عفونی در دوره انتقال حاکی از ناکارآمدی دفاعی سیستم ایمنی به دلیل وضعیت تغییریافته تغذیه ای و متابولیسم مواد مغذی می باشد. بنابراین، درک بهتر از تعاملات چند جانبه بین گاو شیری و ایمنی می تواند به استراتژی های مدیریتی مؤثرتری برای کنترل اختلالات سلامت در پیرامون زمان زایش منجر شود. پژوهش های زیادی نشان دادهاند که تنش متابولیک در زمان حول و حوش زایش در گاوهای شیری ارتباط نزدیکی با اختلال عملکرد چندین مؤلفه پاسخ ایمنی ذاتی و اکتسابی ارتباط دارد.هورمون های خاص مرتبط با زایمان می توانند برخی اثرات نامطلوب بر ایمنی را در زمان حول و حوش زایمان تشریح کنند.
به هر حال، کمبود شدید مواد مغذی ماکرو و میکرو به دلیل نتیجه کاهش DMI و بالانس منفی انرژی، اثر قابل توجهی بر مکانیسم های دفاعی میزبان و اختلالات سلامتی در اوایل شیردهی دارد. فعال سازی پاسخ ایمنی به انرژی نیاز دارد و سیستم ایمنی باید برای مواد مغذی ضروری که برای رشد، رشد ماهیچه و تولید شیر استفاده می شود، رقابت کند.
توسعه و پیشرفت پاسخ های التهابی مزمن و حاد به پاتوژن های عفونی نه تنها باعث آسیب به بافت های میزبان می شود بلکه می تواند مواد مغذی را مجدداً تقسیم نموده و منجر به کاهش قابل ملاحظه رشد و تولید حیوان گردد. بنابراین تعدیل تغذیه دام ها و بهبود مدیریت به منظور کاهش چالش های ایمنولوژیکی می تواند تأثیر مهمی بر بهینه سازی ایمنی و مقاومت بیماری در گاوهای انتقالی شود. از آنجاییکه، آنتی بیوتیک برای درمان بسیاری از بیماری های عفونی به کار می رود، گزینه های درمانی جایگزینی مورد نیاز است تا پاسخ های ایمنی میزبان را هدف قرار دهد. توسعه استراتژی های مبتنی بر تغذیه می تواند موجب بهبود پاسخ ایمنی حیوان شود.
به هر حال، چالش کشف این موضوع است که چگونه بتوانیم پاسخ های مضر میزبان را به طور انتخابی بدون کاهش پاسخ های سودمند که باعث رفع پاتوژن های مهاجم می شوند، را پایین بیاوریم. در مقایسه با داروهای ضد میکروبی که برای درمان بیماری ها در غذای حیوانات استفاده می شود، استراتژی هایی که پاسخ های میزبان را از طریق تغذیه به هدف می رسانند، خطر باقی ماندن دارو و احتمال توسعه پاتوژن های مقاوم به دارو را کاهش می دهد.